Novas descobertas sobre o funcionamento do mal de Alzheimer devem resultar nos próximos cinco anos em medicamentos mais eficientes. Pesquisas cientificas também prometem melhorar o diagnóstico e até reduzir em anos o início do tratamento. E linhas de trabalho caminham para tratamentos parecidos com aqueles aplicados em portadores de diabetes do tipo 2. Sim, o Alzheimer começa a ser chamado na literatura científica de diabetes do tipo 3.
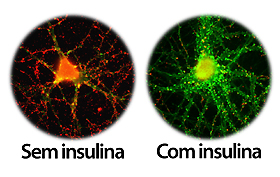
O neurônio sem insulina sofreu perdas da sinapses depois de exposto em laboratório a oligômeros tóxicos (beta amilóide). O neurônio da esquerda foi tratado com insulina e exposto aos oligômeros, permanecendo saudável. Fonte: UFRJ
O Alzheimer é uma doença sem cura e com medicamentos que apenas retardam sua evolução. O diagnóstico, nunca definitivo, é feito após baterias de exames e ressonância magnética, que possam provar a diminuição da função cerebral. Ainda assim, só é possível detectar a doença cerca de oito anos após seu início, quando surgem os primeiros sintomas com os lapsos de memória, que evoluem para a perda da memória de curto prazo, segue para confusão mental, alterações de humor, falhas na linguagem, perda da memória de longo prazo e, por fim, falta de mobilidade e perda da capacidade de se alimentar sozinho.
O fato é que o mal atinge mais de 25 milhões de pessoas no mundo. Acomete 5% da população com mais de 65 anos, e chega a 40% em pessoas com mais de 85 anos. Ainda, segundo dados da Associação Brasileira de Alzheimer (Abraz), o país tem 1,2 milhão de portadores.
A última estimativa divulgada na 11ª Conferência de Pesquisadores da Doença de Alzheimer, realizada em julho deste ano, em Chicago, aponta que em 2040, serão 50 milhões de portadores da doença no mundo. A boa notícia é que novos medicamentos para a doença devem chegar ao mercado entre três e cinco anos, alguns prometendo paralisar o processo de evolução da doença.
Em 2010, cientistas do hospital Toronto Western, em Ontário, Canadá, conseguiram estabilizar e até reverter o processo de perda da massa encefálica em seis pacientes, com um tratamento de estimulação cerebral profunda. Foram implantados no cérebro dos pacientes eletrodos para condução de impulsos elétricos de 130 vezes por segundo na região do hipocampo, responsável pela memória. Após um ano de tratamento o coordenador do trabalho, Andres Lozano, disse em entrevista a New Scientist, que em todos os pacientes houve a reversão do processo de deterioração de neurônios e, em dois casos, aumento do hipocampo em 5% de uma pessoa e em 8% numa outra.
Apesar de trazer esperança, o tratamento deve ser analisado com ressalvas, segundo o pesquisador do departamento de Bioquímica Médica e de Anatomia da Universidade Federal do Rio de Janeiro (UFRJ), Sérgio Teixeira Ferreira. Primeiro, porque poderá não ser eficiente para os primeiros estágios do Alzheimer, quando as sinapses perdem suas funções, mas os neurônios continuam vivos. A segunda razão é que “mesmo que se crie novo neurônio não há garantias que este restabeleça as mesmas conexões sinápticas daquele que estava no mesmo local anteriormente”.
Em entrevista exclusiva dada ao Brasilianas.org, Ferreira, que coordena hoje o desenvolvimento de um remédio que promete impedir a destruição de neurônios, fala das recentes descobertas feitas sobre o funcionamento da doença – que contou com a participação de brasileiros – e sobre o futuro dos medicamentos e diagnósticos mais precisos. A questão, sem dúvida, de saúde pública, preocupa principalmente os dez países com mais idosos no mundo: China, Índia, EUA, Japão, Rússia, Alemanha, Itália, França, Indonésia e Brasil, que juntos possuem 62% da população mundial com mais de 60 anos de idade.
Acompanhe a entrevista.
O tratamento desenvolvido, e ainda em fase de testes, no hospital Toronto Western, Canadá, é promissor?
O que o estudo canadense mostra é uma tentativa de promover uma diminuição, ou mesmo reversão, da perda de massa neuronal [cerebral], numa determinada região do cérebro que é o hipocampo. A premissa, por trás do estudo, é de que a causa da perda de memória no paciente com o mal de Alzheimer é a morte de neurônios. Logo, se existir uma maneira de prevenir a morte, ou até mesmo de fazer nascer novos neurônios, que é o que os autores desse artigo tentam sugerir, a conseqüência será a reversão do prejuízo da perda de memória, ou prejuízo cognitivo. No entanto, acho que essa é uma premissa no mínimo controversa.
Até dez anos atrás era bem aceito na comunidade que o problema de memória em pacientes com Alzheimer era um problema de morte dos neurônios. Nos últimos anos isso tem mudando, estudos, cada vez mais aceitos, propõem que, na verdade, a morte dos neurônios só acontece, realmente, nas fases terminais da doença, quando, de fato, o quadro já é irreversível. Logo, nas fases mais iniciais e mais moderadas da doença, o que acontece é a perda de função das sinapses, que são os pontos de contato entre os neurônios e que permitem que os neurônios conversem entre si. Ou seja, a perda da função da sinapse faz com que o neurônio fique incomunicável. Fazendo uma analogia, imagine que você tenha uma rede de computadores ligados por cabos que permite que eles trabalhem juntos como um grande processador de dados. Se os cabos que ligam o conjunto de computadores forem desinstalados, cada máquina continua viva, mas a função que tinham juntas, de executar o processamento de dados em rede, é comprometida.
Tipicamente, um único neurônio consegue fazer contato com dez mil outros neurônios.Então, no Alzheimer, têm-se uma situação em que as sinapses perderam suas capacidades funcionais normais. Os neurônios continuam vivos, mas não funcionam mais em rede como deveriam para que se forme a memória, para que a pessoa consiga formar um raciocínio abstrato, enfim, qualquer tarefa cognitiva mais complexa. E essa é a visão mais moderna do Alzheimer, da perda de função neuronal, em especial da função sináptica e não necessariamente da morte neuronal. Isso gera, na verdade, um certo otimismo, porque podemos imaginar uma situação em que o paciente começa a ter uma perda de memória, mas os seus neurônios ainda estão vivo. Portanto, a chave agora é talvez impedir ou reverter a disfunção da sinapse, e não tentar ressuscitar os neurônios que estão morrendo, ou criar novos neurônios. Outro problema da estratégia canadense é que mesmo que se crie novo neurônio não há garantias que este restabeleça as mesmas conexões sinápticas daquele que estava no mesmo local anteriormente.
A perda de neurônios está ligada diretamente a falta da utilização dele, por perda de ação das sinapses. Então, a partir daí podemos sugerir a razão da diminuição da massa encefálica, depois de várias fases, justamente porque os neurônios pararam de ser utilizados, por falta da ação das sinapses. É isso?
Sim, é uma sequência que se inicia depois da perda da sinapse. Você pode fazer essa analogia, está menos ativo, então acaba se degenerando.
Já temos esses medicamentos, capazes de melhorar a função das sinapses?
Não, mas existem estudos no Brasil e no exterior com novos medicamentos, inclusive num patamar clínico [com seres humanos]. Na verdade, hoje em dia no mercado, há apenas duas classes de medicamentos aprovados clinicamente para o tratamento do Alzheimer. A primeira classe que surgiu no começo dos anos 1990 são os chamados inibidores de acetilcolinesterase, uma enzima que está presente no cérebro e geralmente degrada uma substância importante chamada acetilcolina, uma molécula de comunicação entre os neurônios. Os níveis de acetilcolina e a comunicação através da acetilcolina são, consequentemente, mais baixos na doença de Alzheimer.
A partir dessa descoberta, se imaginou que inibindo a enzima [acetilcolinesterase] seria possível prolongar a vida média da acetilcolina e resolver o Alzheimer. Existem já várias gerações de medicamentos com essa função na praça, mas a verdade é que nenhum deles realmente melhorou o problema. Na melhor das hipóteses retardam a evolução da doença, e, mesmo assim, só metade dos pacientes respondem a esse tipo de remédio. E, depois de cerca de um ano, o medicamento tende a perder a sua eficácia.
A segunda classe de medicamentos, a memantina, age para proteger os neurônios dos radicais livres que são produzidos na doença de Alzheimer, do chamado estresse oxidativo. O remédio tenta bloquear a ação toxica desses radicais livres produzidos no cérebro do paciente e que podem levar a perda de função e, eventualmente, a morte dos neurônios. Porém, da mesma forma que os tais inibidores de acetilcolinesterase, a memantina também só funciona para alguns pacientes e por um tempo moderado. Diminui a velocidade da doença, mas o paciente vai acabar da mesma forma que outro paciente que nunca tomou o remédio. Pode-se dizer que, dessa forma, não existem no momento medicamentos aprovados para o mal de Alzheimer.
Quais são as apostas para o futuro?
Descobriu-se ao longo dos últimos dez anos que as moléculas, as toxinas que causam a doença de Alzheimer, essa perda de memória, são pequenos agregados de proteínas chamados oligômeros beta amilóides. Esses oligômeros se ligam e atacam as sinapses, ou seja, os pontos de contato entre os neurônios que mencionei anteriormente. E, assim, são capazes de impedir a função das sinapses, bloqueando a conversa entre os neurônios, portanto, o funcionamento da rede neuronal. Tudo isso, leva a perda de memória e de todos os domínios cognitivos.
Existem algumas estratégias que estão sendo imaginadas a partir dessa situação. Uma delas é tentar, por exemplo, bloquear esses oligômeros e atacar a causa, diretamente, e não as consequências da doença, como a memantina e os inibidores de acetilcolinesterase tentam fazer, sem sucesso.
Uma estratégia bastante interessante, e já em testes clínicos, são vacinas, ou anticorpos, que se dirigem especificamente aos oligômeros de beta amilóide. Essa é uma área, sem resultados conclusivos, ainda, mas que em laboratório e em animais está indo muito bem. Existem industrias farmacêuticas perseguindo isso com muito interesse, porque se você tem um anticorpo que é capaz de neutralizar esses oligômeros, então tem uma arma potencialmente poderosa e útil para a doença de Alzheimer.
Outro desdobramento, que pessoalmente acho muito interessante, é uma área que nosso grupo [departamento de Bioquímica Médica e de Anatomia da UFRJ] tem contribuído bastante. Há cerca de uma década foi descoberta a associação entre pacientes com doença de Alzheimer e pacientes diabéticos. Na prática o que se via era que numa população de diabéticos existia maior incidência da doença de Alzheimer, e na população de Alzheimer uma maior incidência de diabéticos do que na população normal. Mas ainda não se conhecia a razão disso. Até que integrantes do nosso grupo aqui no Brasil [Fernanda De Falice, Marcelo Vieira, Theresa Bomfim e Helena Decker, ao lado do professor Sergio Ferreira], em colaboração com grupo de pesquisa dos Estados Unidos, mostraram em artigos publicados em 2008 e 2009, que os oligômeros de beta amilóide também promovem a perda dos receptores de insulina que existem nas sinapses. Até então, classicamente, pensávamos em diabetes como uma doença do pâncreas que afeta o músculo, o tecido adiposo, que afeta o corpo em geral, mas ninguém imaginava que a diabetes poderia ser uma doença do cérebro. Surpreendentemente descobriu-se que os neurônios têm receptores para a insulina, que é o hormônio que controla os níveis de glicose (açúcar) no sangue. Só que nos neurônios essa insulina não funciona para regular a quantidade de açúcar no cérebro, mas para regular a memória e a sobrevivência dos neurônios.
O cérebro, em outras palavras, não é imune a insulina. Pelo contrário, os neurônios precisam do hormônio para formar a memória e também para sobreviver. A insulina tem funções essenciais no sistema nervoso central, no cérebro. E o que a gente mostrou em trabalhos que produzimos nos últimos anos, é que o oligômero de beta amilóide removem ou causam uma eliminação da insulina nos neurônios. Então, mesmo que exista insulina, o neurônio não responde a ela, parecido com o que acontece no diabetes do tipo 2, quando o paciente produz a insulina no pâncreas, mas seu músculo, ou tecido adiposo, não responde a insulina, porque o receptor dela não está lá.
A partir desses estudos, o Alzheimer passa a ser visto como uma espécie de diabetes cerebral, Já está surgindo na literatura científica a menção do diabetes do tipo 3, que seria justamente esse diabetes cerebral associado à doença de Alzheimer. Para mim isso é muito excitante porque abre a perspectiva de que futuramente a gente possa desenvolver novos tratamentos para a doença que sejam baseados no que já conhecemos hoje como mecanismos de tratamento para o diabetes.
E quais são as novas fronteiras em relação ao diagnóstico do Alzheimer?
Essa é uma questão fundamental e, como disse antes, o problema é que nas fases iniciais da doença você tem a perda de memória, mas os neurônios estão vivos. Logo, assim que conseguimos detectar a doença, podendo entrar com a intervenção o quanto antes, torna-se possível interromper esse processo. Agora, se o diagnóstico chegar tarde demais, numa fase mais avançada do processo de perda de neurônios, a situação é praticamente irreversível.
Entretanto, ainda hoje, o diagnóstico que chamamos de definitivo da doença de Alzheimer é aquele feito após a morte, pela análise do cérebro na necropsia. Atualmente, existem várias ferramentas que, juntas, levam a uma grande confiança de que o paciente tem de fato o Alzheimer. São feitos exames de neuroimagem, ou de ressonância magnética, onde é possível examinar o tamanho do hipocampo do paciente, região do cérebro associada a formação inicial da memória, e ver se está se atrofiando ou não. Existem, ainda baterias de testes neuropsicológicos que as pessoas respondem, executam diferentes funções, tarefas, evocação de palavras, cálculos e desenhos que podem levar a um diagnóstico provável.
Nosso grupo de estudos está interessado numa linha de investigação para melhorar o diagnóstico e tentar identificar precocemente alterações nos níveis daqueles oligômeros de beta amilóide no nosso cérebro. Através da dosagem desses agregados de proteínas, que são as toxinas que elevam a perda de função e de memória, poderemos diagnosticar o mais cedo possível o mal.
Como seria o procedimento médico de medição dessas toxinas no cérebro?
Através do exame de liquor, que é o líquido no qual nosso cérebro está imerso e que também circula pela medula. Da mesma forma de quando você tem uma meningite, por exemplo, faz um exame do liquor e isso é coletado por uma pulsão feita na medula. Então é possível com a análise do liquor tentar ver os níveis de oligômeros. Isso é algo que outros grupos no mundo, inclusive o nosso, estão tentando fazer.
Num futuro breve, uma pessoa que quiser ver se tem tendência a ter o mal de Alzheimer, por questões familiares, por exemplo, vai poder fazer esse exame periodicamente?
Os casos familiares da doença respondem por, no máximo, 10% dos casos do Alzheimer. Então, não é uma doença transmitida geneticamente de forma massiva, como se pode imaginar. Não é porque seu avô, ou mesmo seu pai teve, que você irá ter. E a idade típica para se desenvolver a doença, como você já sabe, é acima dos 65 anos no geral, que respondem por mais de 90% dos pacientes.
Quanto aos exames, não diria que serão feitos periodicamente, mas a partir dos lapsos de memória mais frequentes do que o normal. Porque todo mundo tem lapsos de memória, eventuais, faz parte do cérebro esquecer coisas, e isso é até bom, gravamos o que consideramos importantes. Mas quando os lapsos de memória começam a prejudicar o paciente, ele deve ser submetido a uma bateria de exames neuropsicológicos, de sangue, de ressonância magnética por imagem, vários exames que podem levar a um diagnóstico muito possível de Alzheimer. Nesse caso, quando tivermos, no futuro, um teste mais fidedigno, bem sensível que detecte os oligômeros de beta amilóide no liquor, aí sim essa pessoa vai ser indicada para fazer o restante dos exames.
Já teríamos indícios de que tipo de medicamentos podem ser utilizados para impedir a ação dessas toxinas?
Sou um pouco tendencioso, nesse sentido, porque uma questão muito importante é essa questão do diabetes. Saiu, por exemplo, na mesma revista desse artigo canadense [New Scientist], agora há dois meses, talvez, o artigo da Suzanne Craft [do Department of Veterans Affair/AV]. A cientista mostra um ensaio clínico com cerca de cem pacientes, voluntários, uma metade diagnosticada com Alzheimer, outra não. Eles receberam insulina por via intranasal, que é uma forma de fazer a insulina chegar mais rápido ao cérebro. Ela reporta melhoras cognitivas desses pacientes com estágio ainda inicial do mal de Alzheimer. E esse trabalho dela, justamente, cita muito os nossos trabalhos, porque a partir dessa ideia de que o Alzheimer seria uma forma de diabetes ela se inspirou para buscar uma forma de tratamento. Nossos estudos foram todos feitos em laboratório, mas ela já está conseguindo fazer com pacientes a administração de insulina intranasal, trazendo melhoras. Ainda é piloto com um número reduzido de pacientes, mas acho muito promissor. Então visualizo que esse será o caminho dos novos tratamentos nos próximos anos.
As pessoas com baixa escolaridade têm tendência a desenvolver um pouco mais cedo o mal?
Essa é uma questão um pouco controversa. Existem alguns estudos que sugerem essa reserva cognitiva, de que pessoas que utilizam mais seu cérebro estão mais protegidas. Assim como tem outros estudos que dizem que isso não se comprova. Mas não sei exatamente o que dizer sobre isso, porque a literatura sobre o tema é muito controversa.
*O bioquímico Sérgio Teixeira Ferreira coordena, no departamento de Bioquímica Médica e de Anatomia da UFRJ, pesquisa de uma nova droga criada a partir de dois compostos orgânicos e que impedem a destruição dos neurônios.
Novas descobertas sobre o funcionamento do mal de Alzheimer devem resultar nos próximos cinco anos em medicamentos mais eficientes. Pesquisas cientificas também prometem melhorar o diagnóstico e até reduzir em anos o início do tratamento. E linhas de trabalho caminham para tratamentos parecidos com aqueles aplicados em portadores de diabetes do tipo 2. Sim, o mal de Alzheimer começa a ser chamado na literatura científica de diabetes do tipo 3.
O mal de Alzheimer é uma doença sem cura e com medicamentos que apenas retardam sua evolução. O diagnóstico, nunca definitivo, é feito após baterias de exames e ressonância magnética, que possam provar a diminuição da função cerebral. Ainda assim, só é possível detectar a doença cerca de oito anos após seu início, quando surgem os primeiros sintomas com os lapsos de memória, que evoluem para a perda da memória de curto prazo, segue para confusão mental, alterações de humor, falhas na linguagem, perda da memória de longo prazo e, por fim, falta de mobilidade e perda da capacidade de se alimentar sozinho.
O fato é que o mal atinge mais de 25 milhões de pessoas no mundo. Acomete 5% da população com mais de 65 anos, e chega a 40% em pessoas com mais de 85 anos. Ainda, segundo dados da Associação Brasileira de Alzheimer (Abraz), o país tem 1,2 milhão de portadores.
A última estimativa divulgada na 11ª Conferência de Pesquisadores da Doença de Alzheimer, realizada em julho deste ano, em Chicago, aponta que em 2040, serão 50 milhões de portadores da doença no mundo. A boa notícia é que novos medicamentos para a doença devem chegar ao mercado entre três e cinco anos, alguns prometendo paralisar o processo de evolução da doença.
Em 2010, cientistas do hospital Toronto Western, em Ontário, Canadá, conseguiu estabilizar e até reverter o processo de massa cerebral em seis pacientes, com um tratamento de estimulação cerebral profunda. Foram implantados no cérebro dos pacientes eletrodos para condução de impulsos elétricos de 130 vezes por segundo. Após um ano de tratamento o coordenador do trabalho, Andres Lozano, disse em entrevista a New Scientist, que em todos os pacientes houve a reversão do processo de deterioração de neurônios e, em dois casos, aumento do hipocampo, responsável pela memória, em 5% de uma pessoa, e em 8% numa outra.
Apesar de trazer esperança, o tratamento deve ser analisado com ressalvas, segundo o pesquisador do departamento de Bioquímica Médica e de Anatomia da Universidade Federal do Rio de Janeiro (UFRJ), Sérgio Teixeira Ferreira. Primeiro, porque poderá não ser eficiente para os primeiros estágios do Alzheimer, quando as sinapses perdem suas funções, mas os neurônios continuam vivos. A segunda razão é que “mesmo que se crie novo neurônio não há garantias que este restabeleça as mesmas conexões sinápticas daquele que estava no mesmo local anteriormente”.
Em entrevista exclusiva dada ao Brasilianas.org, Ferreira, que coordena hoje o desenvolvimento de um remédio que promete impedir a destruição de neurônios, fala das recentes descobertas feitas sobre o funcionamento da doença – que contou com a participação de brasileiros – e sobre o futuro dos medicamentos e diagnósticos mais precisos. A questão, sem dúvida, de saúde pública, preocupa principalmente os dez países com mais idosos no mundo: China, Índia, EUA, Japão, Rússia, Alemanha, Itália, França, Indonésia e Brasil, que juntos possuem 62% da população mundial com mais de 60 anos de idade.
O neurônio sem insulina sofreu perdas da sinapses depois de exposto em laboratório a oligômeros tóxicos (beta amilóide). O neurônio da esquerda foi tratado com insulina e exposto aos oligômeros, permanecendo saudável. Fonte: UFRJ
Acompanhe a entrevista.
O tratamento desenvolvido, e ainda em fase de testes, no hospital Toronto Western, Canadá é promissor?
O que o estudo canadense mostra é uma tentativa de promover uma diminuição, ou mesmo reversão, da perda de massa neuronal [cerebral], numa determinada região do cérebro que é o hipocampo. A premissa, por trás do estudo, é de que a causa da perda de memória no paciente com o mal de Alzheimer é a morte de neurônios. Logo, se existir uma maneira de prevenir a morte, ou até mesmo de fazer nascer novos neurônios, que é o que os autores desse artigo tentam sugerir, a conseqüência será a reversão do prejuízo da perda de memória, ou prejuízo cognitivo. No entanto, acho que essa é uma premissa no mínimo controversa.
Até dez anos atrás era bem aceito na comunidade que o problema de memória em pacientes com Alzheimer era um problema de morte dos neurônios. Nos últimos anos isso tem mudando, estudos, cada vez mais aceitos, propõem que, na verdade, a morte dos neurônios só acontece, realmente, nas fases terminais da doença, quando, de fato, o quadro já é irreversível. Logo, nas fases mais iniciais e mais moderadas da doença, o que acontece é a perda de função das sinapses, que são os pontos de contato entre os neurônios e que permitem que os neurônios conversem entre si. Ou seja, a perda da função da sinapse faz com que o neurônio fique incomunicável. Fazendo uma analogia, imagine que você tenha uma rede de computadores ligados por cabos que permite que eles trabalhem juntos como um grande processador de dados. Se os cabos que ligam o conjunto de computadores forem desinstalados, cada máquina continua viva, mas a função que tinham juntas, de executar o processamento de dados em rede, é comprometida.
Tipicamente, um único neurônio consegue fazer contato com dez mil outros neurônios.Então, no Alzheimer, têm-se uma situação em que as sinapses perderam suas capacidades funcionais normais. Os neurônios continuam vivos, mas não funcionam mais em rede como deveriam para que se forme a memória, para que a pessoa consiga formar um raciocínio abstrato, enfim, qualquer tarefa cognitiva mais complexa. E essa é a visão mais moderna do Alzheimer, da perda de função neuronal, em especial da função sináptica e não necessariamente da morte neuronal. Isso gera, na verdade, um certo otimismo, porque podemos imaginar uma situação em que o paciente começa a ter uma perda de memória, mas os seus neurônios ainda estão vivo. Portanto, a chave agora é talvez impedir ou reverter a disfunção da sinapse, e não tentar ressuscitar os neurônios que estão morrendo, ou criar novos neurônios. Outro problema da estratégia canadense é que mesmo que se crie novo neurônio não há garantias que este restabeleça as mesmas conexões sinápticas daquele que estava no mesmo local anteriormente.
A perda de neurônios está ligada diretamente a falta da utilização dele, por perda de ação das sinapses. Então, a partir daí podemos sugerir a razão da diminuição da massa encefálica, depois de várias fases, justamente porque os neurônios pararam de ser utilizados, por falta da ação das sinapses. É isso?
Sim, é uma sequência que se inicia depois da perda da sinapse. Você pode fazer essa analogia, está menos ativo, então acaba se degenerando.
Já temos esses medicamentos, capazes de melhorar a função das sinapses?
Não, mas existem estudos no Brasil e no exterior com novos medicamentos, inclusive num patamar clínico [com seres humanos]. Na verdade, hoje em dia no mercado, há apenas duas classes de medicamentos aprovados clinicamente para o tratamento do Alzheimer. A primeira classe que surgiu no começo dos anos 1990 são os chamados inibidores de acetilcolinesterase, uma enzima que está presente no cérebro e geralmente degrada uma substância importante chamada acetilcolina, uma molécula de comunicação entre os neurônios. Os níveis de acetilcolina e a comunicação através da acetilcolina são, consequentemente, mais baixos na doença de Alzheimer.
A partir dessa descoberta, se imaginou que inibindo a enzima [acetilcolinesterase] seria possível prolongar a vida média da acetilcolina e resolver o Alzheimer. Existem já várias gerações de medicamentos com essa função na praça, mas a verdade é que nenhum deles realmente melhorou o problema. Na melhor das hipóteses retardam a evolução da doença, e, mesmo assim, só metade dos pacientes respondem a esse tipo de remédio. E, depois de cerca de um ano, o medicamento tende a perder a sua eficácia.
A segunda classe de medicamentos, a memantina, age para proteger os neurônios dos radicais livres que são produzidos na doença de Alzheimer, do chamado estresse oxidativo. O remédio tenta bloquear a ação toxica desses radicais livres produzidos no cérebro do paciente e que podem levar a perda de função e, eventualmente, a morte dos neurônios. Porém, da mesma forma que os tais inibidores de acetilcolinesterase, a memantina também só funciona para alguns pacientes e por um tempo moderado. Diminui a velocidade da doença, mas o paciente vai acabar da mesma forma que outro paciente que nunca tomou o remédio. Pode-se dizer que, dessa forma, não existem no momento medicamentos aprovados para o mal de Alzheimer.
Quais são as apostas para o futuro?
Descobriu-se ao longo dos últimos dez anos que as moléculas, as toxinas que causam a doença de Alzheimer, essa perda de memória, são pequenos agregados de proteínas chamados oligômeros beta amilóides. Esses oligômeros se ligam e atacam as sinapses, ou seja, os pontos de contato entre os neurônios que mencionei anteriormente. E, assim, são capazes de impedir a função das sinapses, bloqueando a conversa entre os neurônios, portanto, o funcionamento da rede neuronal. Tudo isso, leva a perda de memória e de todos os domínios cognitivos.
Existem algumas estratégias que estão sendo imaginadas a partir dessa situação. Uma delas é tentar, por exemplo, bloquear esses oligômeros e atacar a causa, diretamente, e não as consequências da doença, como a memantina e os inibidores de acetilcolinesterase tentam fazer, sem sucesso.
Uma estratégia bastante interessante, e já em testes clínicos, são vacinas, ou anticorpos, que se dirigem especificamente aos oligômeros de beta amilóide. Essa é uma área, sem resultados conclusivos, ainda, mas que em laboratório e em animais está indo muito bem. Existem industrias farmacêuticas perseguindo isso com muito interesse, porque se você tem um anticorpo que é capaz de neutralizar esses oligômeros, então tem uma arma potencialmente poderosa e útil para a doença de Alzheimer.
Outro desdobramento, que pessoalmente acho muito interessante, é uma área que nosso grupo [departamento de Bioquímica Médica e de Anatomia da UFRJ] tem contribuído bastante. Há cerca de uma década foi descoberta a associação entre pacientes com doença de Alzheimer e pacientes diabéticos. Na prática o que se via era que numa população de diabéticos existia maior incidência da doença de Alzheimer, e na população de Alzheimer uma maior incidência de diabéticos do que na população normal. Mas ainda não se conhecia a razão disso. Até que integrantes do nosso grupo aqui no Brasil [Fernanda De Falice, Marcelo Vieira, Theresa Bomfim e Helena Decker, ao lado do professor Sergio Ferreira], em colaboração com grupo de pesquisa dos Estados Unidos, mostraram em artigos publicados em 2008 e 2009, que os oligômeros de beta amilóide também promovem a perda dos receptores de insulina que existem nas sinapses. Até então, classicamente, pensávamos em diabetes como uma doença do pâncreas que afeta o músculo, o tecido adiposo, que afeta o corpo em geral, mas ninguém imaginava que a diabetes poderia ser uma doença do cérebro. Surpreendentemente descobriu-se que os neurônios têm receptores para a insulina, que é o hormônio que controla os níveis de glicose (açúcar) no sangue. Só que nos neurônios essa insulina não funciona para regular a quantidade de açúcar no cérebro, mas para regular a memória e a sobrevivência dos neurônios.
O cérebro, em outras palavras, não é imune a insulina. Pelo contrário, os neurônios precisam do hormônio para formar a memória e também para sobreviver. A insulina tem funções essenciais no sistema nervoso central, no cérebro. E o que a gente mostrou em trabalhos que produzimos nos últimos anos, é que o oligômero de beta amilóide removem ou causam uma eliminação da insulina nos neurônios. Então, mesmo que exista insulina, o neurônio não responde a ela, parecido com o que acontece no diabetes do tipo 2, quando o paciente produz a insulina no pâncreas, mas seu músculo, ou tecido adiposo, não responde a insulina, porque o receptor dela não está lá.
A partir desses estudos, o Alzheimer passa a ser visto como uma espécie de diabetes cerebral, Já está surgindo na literatura científica a menção do diabetes do tipo 3, que seria justamente esse diabetes cerebral associado à doença de Alzheimer. Para mim isso é muito excitante porque abre a perspectiva de que futuramente a gente possa desenvolver novos tratamentos para a doença que sejam baseados no que já conhecemos hoje como mecanismos de tratamento para o diabetes.
E quais são as novas fronteiras em relação ao diagnóstico do Alzheimer?
Essa é uma questão fundamental e, como disse antes, o problema é que nas fases iniciais da doença você tem a perda de memória, mas os neurônios estão vivos. Logo, assim que conseguimos detectar a doença, podendo entrar com a intervenção o quanto antes, torna-se possível interromper esse processo. Agora, se o diagnóstico chegar tarde demais, numa fase mais avançada do processo de perda de neurônios, a situação é praticamente irreversível.
Entretanto, ainda hoje, o diagnóstico que chamamos de definitivo da doença de Alzheimer é aquele feito após a morte, pela análise do cérebro na necropsia. Atualmente, existem várias ferramentas que, juntas, levam a uma grande confiança de que o paciente tem de fato o Alzheimer. São feitos exames de neuroimagem, ou de ressonância magnética, onde é possível examinar o tamanho do hipocampo do paciente, região do cérebro associada a formação inicial da memória, e ver se está se atrofiando ou não. Existem, ainda baterias de testes neuropsicológicos que as pessoas respondem, executam diferentes funções, tarefas, evocação de palavras, cálculos e desenhos que podem levar a um diagnóstico provável.
Nosso grupo de estudos está interessado numa linha de investigação para melhorar o diagnóstico e tentar identificar precocemente alterações nos níveis daqueles oligômeros de beta amilóide no nosso cérebro. Através da dosagem desses agregados de proteínas, que são as toxinas que elevam a perda de função e de memória, poderemos diagnosticar o mais cedo possível o mal.
Como seria o procedimento médico de medição dessas toxinas no cérebro?
Através do exame de liquor, que é o líquido no qual nosso cérebro está imerso e que também circula pela medula. Da mesma forma de quando você tem uma meningite, por exemplo, você faz um exame do liquor e isso é coletado por uma pulsão feita na medula. Então é possível com a análise do liquor tentar ver os níveis de oligômeros. Isso é algo que outros grupos no mundo, inclusive o nosso, estão tentando fazer.
Num futuro breve, uma pessoa que quiser ver se tem tendência a ter o mal de Alzheimer, por questões familiares, por exemplo, vai poder fazer esse exame periodicamente?
Os casos familiares da doença respondem por, no máximo, 10% dos casos do Alzheimer. Então, não é uma doença transmitida geneticamente de forma massiva, como se pode imaginar. Não é porque seu avô, ou mesmo seu pai teve, que você irá ter. E a idade típica para se desenvolver a doença, como você já sabe, é acima dos 65 anos no geral, que respondem por mais de 90% dos pacientes.
Quanto aos exames, não diria que serão feitos periodicamente, mas a partir dos lapsos de memória mais frequentes do que o normal. Porque todo mundo tem lapsos de memória, eventuais, faz parte do cérebro esquecer coisas, e isso é até bom, gravamos o que consideramos importantes. Mas, quando os lapsos de memória começam a prejudicar o paciente, ele deve ser submetido a uma bateria de exames neuropsicológicos, de sangue, de ressonância magnética por imagem, vários exames que podem levar a um diagnóstico muito possível de Alzheimer. Nesse caso, quando tivermos, no futuro, um teste mais fidedigno, bem sensível que detecte os oligômeros de beta amilóide no liquor, aí sim essa pessoa vai ser indicada para fazer o restante dos exames.
Já teríamos indícios de que tipo de medicamentos podem ser utilizados para impedir a ação dessas toxinas?
Sou um pouco tendencioso, nesse sentido, porque uma questão muito importante é essa questão do diabetes. Saiu, por exemplo, na mesma revista desse artigo canadense [New Scientist], agora há dois meses, talvez, o artigo da Suzanne Craft [do Department of Veterans Affair/AV]. A cientista mostra um ensaio clínico com cerca de cem pacientes, voluntários, uma metade diagnosticada com Alzheimer, outra não. Eles receberam insulina por via intranasal, que é uma forma de fazer a insulina chegar mais rápido ao cérebro. Ela reporta melhoras cognitivas desses pacientes com estágio ainda inicial do mal de Alzheimer. E esse trabalho dela, justamente, cita muito os nossos trabalhos, porque a partir dessa ideia de que o Alzheimer seria uma forma de diabetes ela se inspirou para buscar uma forma de tratamento. Nossos estudos foram todos feitos em laboratório, mas ela já está conseguindo fazer com pacientes a administração de insulina intranasal, trazendo melhoras. Ainda é piloto com um número reduzido de pacientes, mas acho muito promissor. Então visualizo que esse será o caminho dos novos tratamentos nos próximos anos.
As pessoas com baixa escolaridade têm tendência a desenvolver um pouco mais cedo o mal?
Essa é uma questão um pouco controversa. Existem alguns estudos que sugerem essa reserva cognitiva, de que pessoas que utilizam mais seu cérebro estão mais protegidas. Assim como tem outros estudos que dizem que isso não se comprova. Mas não sei exatamente o que dizer sobre isso, porque a literatura sobre o tema é muito controversa, ainda.
*O bioquímico Sérgio Teixeira Ferreira coordena, no departamento de Bioquímica Médica e de Anatomia da UFRJ, pesquisa de uma nova droga criada a partir de dois compostos orgânicos e que impedem a destruição dos neurônios.
Você pode fazer o Jornal GGN ser cada vez melhor.
Apoie e faça parte desta caminhada para que ele se torne um veículo cada vez mais respeitado e forte.



 produtos
produtos



