O CAR-T Cell, terapia celular contra o câncer, pode obter autorização da Agência Nacional de Vigilância Sanitária (Anvisa) para uso comercial e incorporação no Sistema Único de Saúde (SUS) em até dois anos, se as próximas fases do estudo clínico do tratamento confirmarem os resultados promissores.
No Brasil, o estudo é desenvolvido em parceria pela Universidade de São Paulo (USP), Instituto Butantan e o Hemocentro de Ribeirão Preto. Entre os 14 pacientes submetidos ao tratamento, todos tiveram, pelo menos, 60% de remissão dos tumores, mesmo em quadros em que a doença estava em estágio avançado.
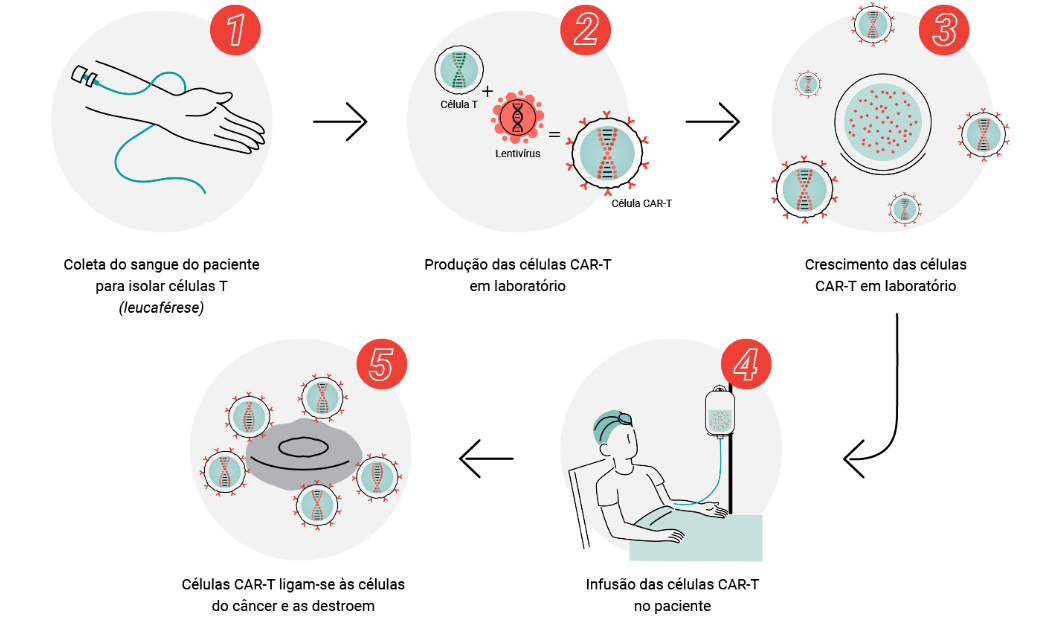
A terapia contra o câncer retira as células T do sistema de defesa do paciente e as modifica geneticamente para que possam reconhecer as células cancerígenas. Reintroduzidas ao corpo, as células T se multiplicam e são capazes de eliminar os tumores.
“A grande vantagem da terapia celular é o fato de que a gente consegue programar a célula para que ela atinja direto as células tumorais”, explica Gustavo Mendes, diretor de Assuntos Regulatórios, Qualidade e Ensaios Clinicos do Instituto Butantan, em entrevista ao GGN.
Pesquisa
Mendes conta à reportagem que o Brasil já tem produtos de terapia celular desde 2021. Em relação à oncologia, o tratamento em estudo é aplicado em três variações: leucemia linfoblástica B, linfoma não Hodgkin de células B e mieloma múltiplo, pois são os tipos de câncer mais difíceis de tratar.
A primeira aplicação do CAR-T Cell fez parte do que o Instituto Butantan chama de uso científico, realizado antes da pesquisa clínica. O próximo passo agora é obter a autorização da Anvisa para o início da pesquisa clínica, em que a expectativa é a liberação em agosto.
Na primeira fase do estudo, composto por três etapas, a terapia será aplicada em uma população de 70 pessoas, em que o objetivo será reproduzir o tratamento com segurança e acompanhamento a longo prazo, a fim de verificar se os pacientes não terão novas manifestações da doença.
Já na segunda fase, amplia-se a quantidade de pacientes. “Vamos otimizar o regime de tratamento, para ver qual é o tratamento mais adequado, a posologia, qual periodicidade, se vai presisar repetir a aplicação ou se é única, a quantidade de células que temos de utilizar”, continua o diretor do Instituto Butantan.
A última fase do estudo almeja a confirmação de resultados do tratamento nas fases anteriores, a partir da aplicação da terapia em uma quantidade de pacientes ainda maior. Apenas depois destas três etapas é que o CAR-T Cell é liberado pela Anvisa para o mercado.
Antecipação
Ainda que a pesquisa clínica tenham três fases, Gustavo Mendes acredita que o tratamento pode obter a liberação para uso comercial em tempo menor.
“Por se tratar de uma terapia bastante inovadora e disruptiva, é possível que a Anvisa já na fase 2 autorize. Então, são cenários otimistas em que a gente tem bons resultados e que a gente consiga comprovar para a Anvisa que vai fazer uma diferença mesmo e a gente conseguiria reduzir o tempo das fases para uso disseminado”, diz o diretor do Butantan.
O efeito colateral do tratamento é um expressivo processo inflamatório, já que as células T rompem as células cancerígenas e todo este conteúdo se espalha pelo organismo.
Esta etapa tem de ser acompanhada pela equipe médica. No mais, não há indicativo de que as células T se incorporam no corpo ou induzem a outros cânceres, de acordo com as experiências já observadas em modelos animais.
Mais desafios
O próximo desafio dos institutos de pesquisa é nacionalizar a produção de todas as etapas do tratamento. Hoje, as células são retiradas do paciente, enviadas ao exterior para a modificação genética, repatriadas e aplicadas no paciente.
Assim, a Câmara de Regulação do Mercado de Medicamentos (CMED) determinou que o preço da terapia celular em R$ 2 milhões, a fim de custear a inovação, o custo das pesquisas e de inovação. Ao nacionalizar toda a tecnologia do tratamento, o investimento tende a ser mais acessível.
Em relação aos demais tipos de câncer, ainda faltam pesquisas específicas para a aplicação das células T em pacientes. Mas Gustavo Mendes adianta que a terapia celular já se mostrou uma boa estratégia de tratamento para pacientes em estágio avançado da doença.
Por se tratar de uma terapia individualizada, o CAR-T Cell pode ser também uma alternativa promissora para o tratamento de doenças autoimunes, como lúpus e artrite.
LEIA TAMBÉM:





Jicxjo
23 de julho de 2023 1:23 pmQue tudo corra como esperado nos testes e a ciência tenha mesmo desenvolvido uma nova técnica eficaz e definitiva contra o câncer. Enquanto continua sendo de alto custo, há de se começar pelos pacientes graves e com metástases fora de controle, mas é uma questão de tempo para que se vá tornando mais e mais acessível. Parabéns a todos os envolvidos nessa pesquisa!